Forskningsblogg
Nervsystemet
Publicerad 2020-05-26
En traumatisk ryggmärgsskada innebär att ryggmärgen skadas och helt eller delvis går av.
För att förstå vad detta får för konsekvenser i kroppen kommer vi här gå igenom hur nervsystemet och ryggmärgen är uppbyggt och vad som gör att ryggmärgen inte kan läka.
Centrala och perifera nervsystemet
Kroppens nervsystem delas in i det centrala och det perifera nervsystemet. Det centrala består av hjärnan och ryggmärgen och det perifera nervsystemet består av nervtrådar som går ut från hjärnan och ryggmärgen till kroppens olika delar.
Nervsystemets uppgift är att ta emot och att förmedla signaler från och till kroppens olika delar. Det gör att kroppens olika delar kan samarbeta. Nervsystemet styr våra sinnen; känsel, lukt, hörsel och syn. Det gör att vi kan utföra viljemässiga rörelser och ansvarar för att vi har ett medvetande, kan uppleva känslor och att vi kan minnas saker.
Det centrala nervsystemet är uppbyggt av ca 100 miljoner nervceller (neuron) och ungefär lika många stödjande gliaceller.
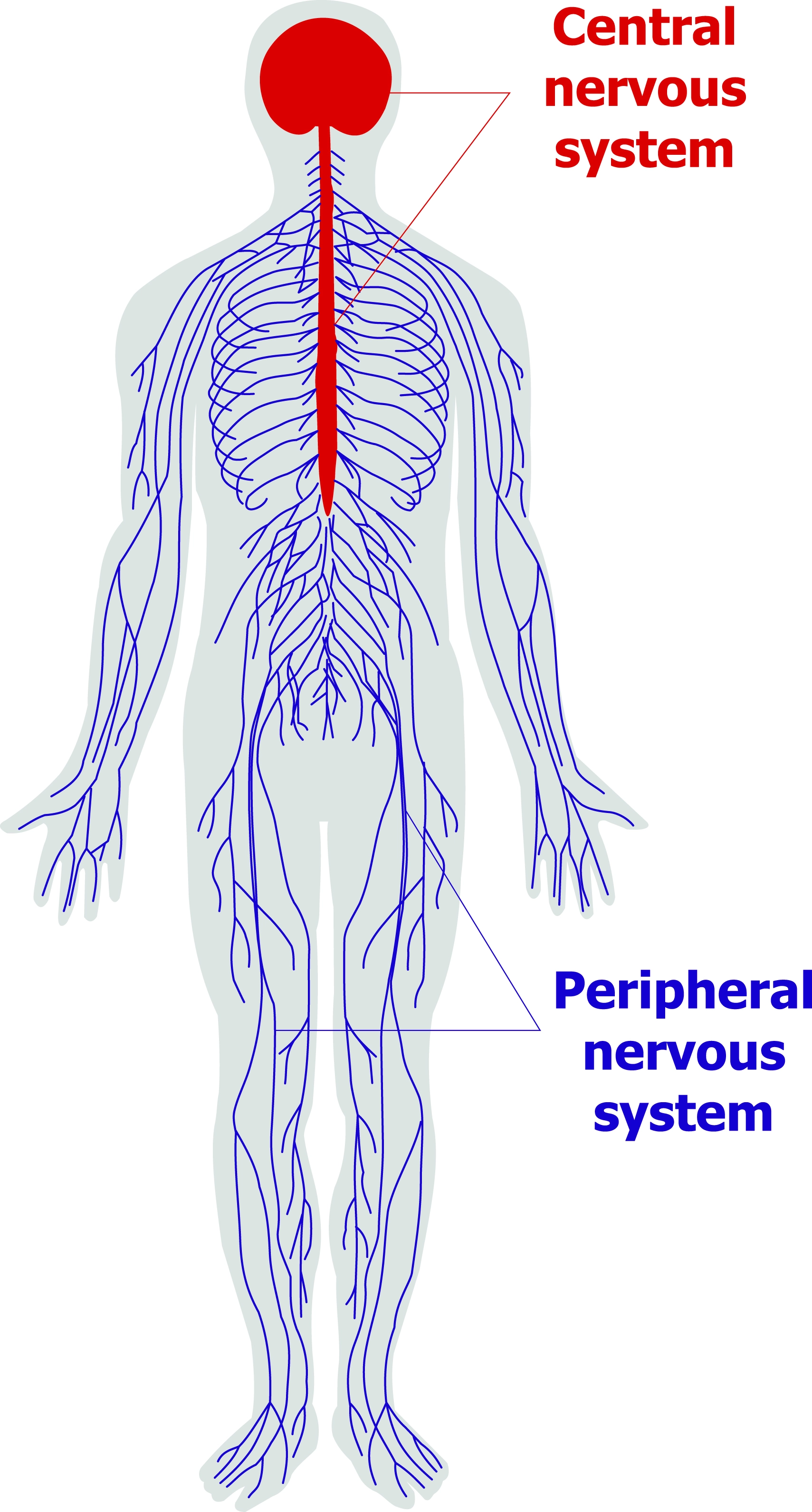
Centrala och perifera nervsystemet
Nervcellen
Nervcellen är uppbyggd på liknande sätt som andra celler i kroppen. Den har en cellkärna och olika delar som fyller olika funktioner i cellen. En sak som skiljer nervcellen från andra celler i kroppen är att den inte delar sig och förnyas i den vuxna kroppen.
En annan sak som som skiljer den från andra celler är att den har trådliknande utskott, som kallas axon.
Axonet leder elektriska signaler ut från nervcellen. Nervcellen har också flera kortare nervtrådar som kallas dendriter, som leder signaler in till cellen. Signalerna sprids i nervcellen, ut genom axonet och vidare till andra nervceller, muskler eller körtlar. En nervcell kan ha kontakt med mer än tusen andra nervceller och kan kontaktas av ytterligare tusen andra celler. På så sätt bildas ett komplext nätverk av celler.
De längsta nervtrådarna är över en meter långa och finns i ischiasnerven i benet.
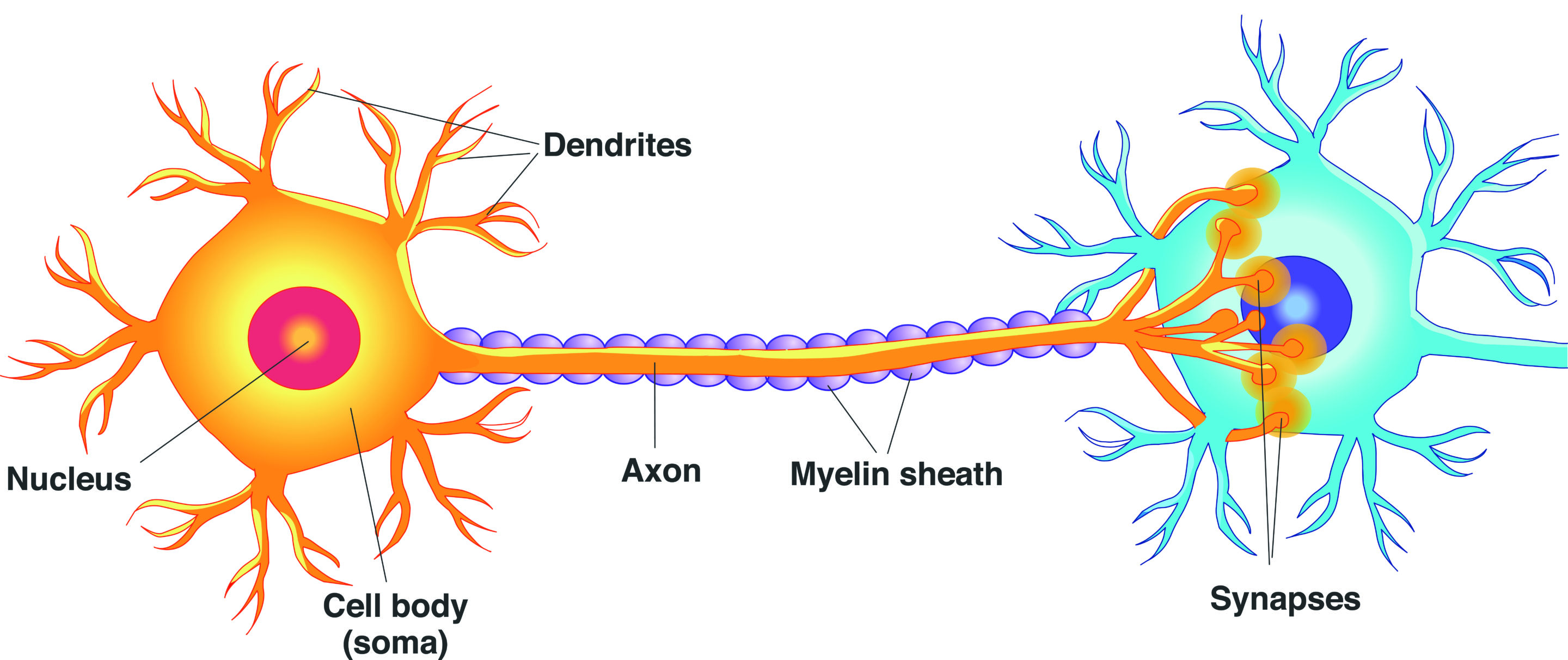
Nervcellen
Myelin
En del nervtrådar omges av ett skydd som kallas myelinskida. Myelinet består av fett och fungerar som isolering och skydd för nervtråden. Myelinet täcker inte hela nerven, utan det finns små mellanrum som kallas noder.
Nerver med myelinskida leder signaler snabbare än nerver utan myelinskida. Det beror på att signalen hoppar mellan noderna.
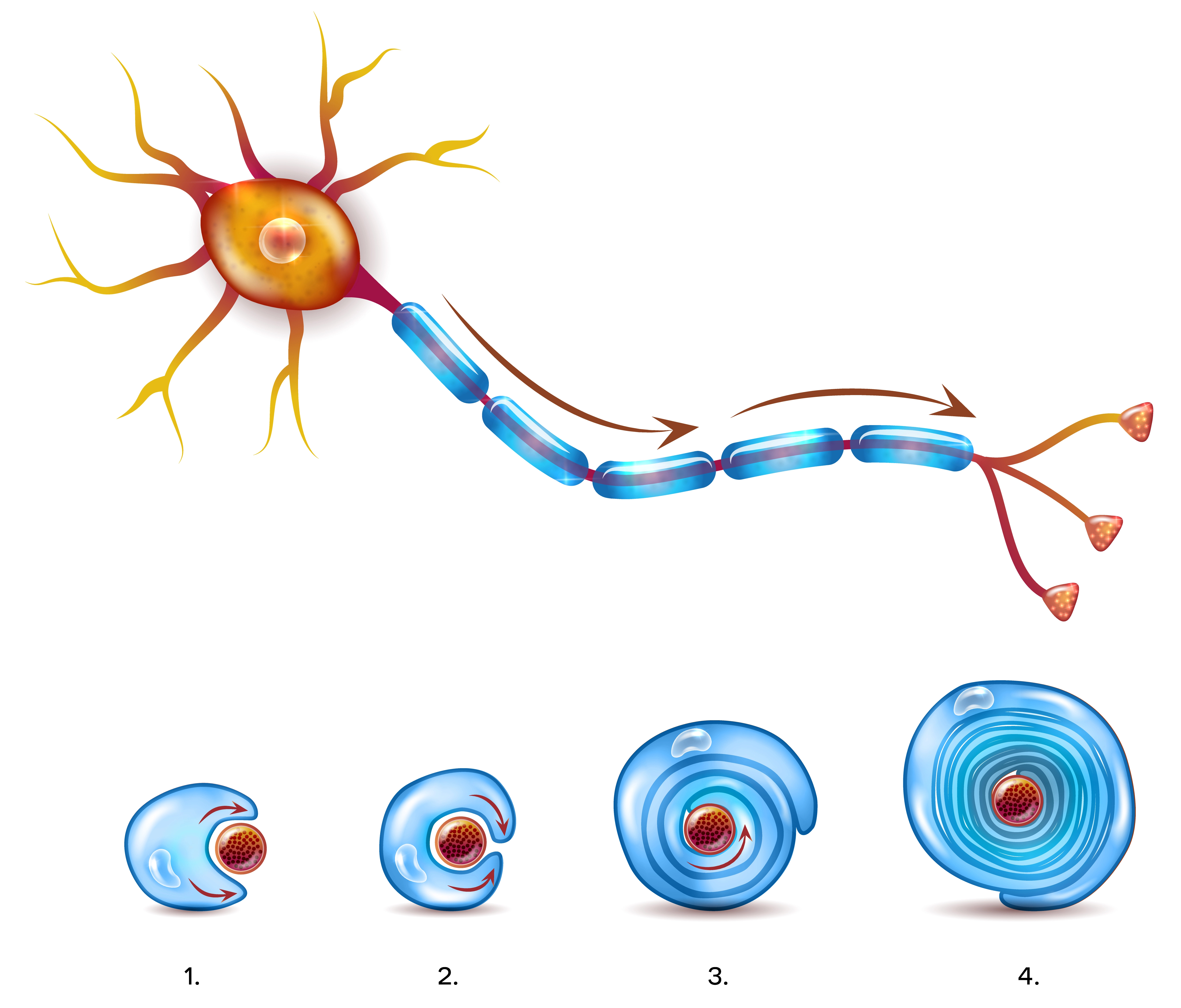
Myelin
Synapsen
En synaps är den plats – ett mellanrum – där en nervcell kontaktar en annan cell. Synapser kan finnas mellan två nervceller, mellan en nervcell och en muskelcell, eller mellan en nervcell och en körtelcell. I synapsen kommunicerar en nervcell med nästa cell genom att frisätta ämnen kallade signalsubstanser som fäster på receptorer på nästa cell. En del läkemedel fungerar genom att blockera receptorerna så att signalsubstansen inte kan fästa – och signalen hindras då från att nå fram.
På den nervcell som avger en signalsubstans finns även receptorer som återupptar signalsubstansen till samma cell – för att reglera nivån av aktiv substans. En del läkemedel blockerar dessa återupptagningsreceptorer så att signalsubstansen inte kan återupptas – vilket leder till en förhöjd nivå av den aktiva substansen. Ett exempel på en sådan medicin är antidepressiva läkemedel som SSRI (som gått under namn som Prozac eller “lyckopiller” i folkmun.) Det höjer nivån av signalsubstansen serotonin.
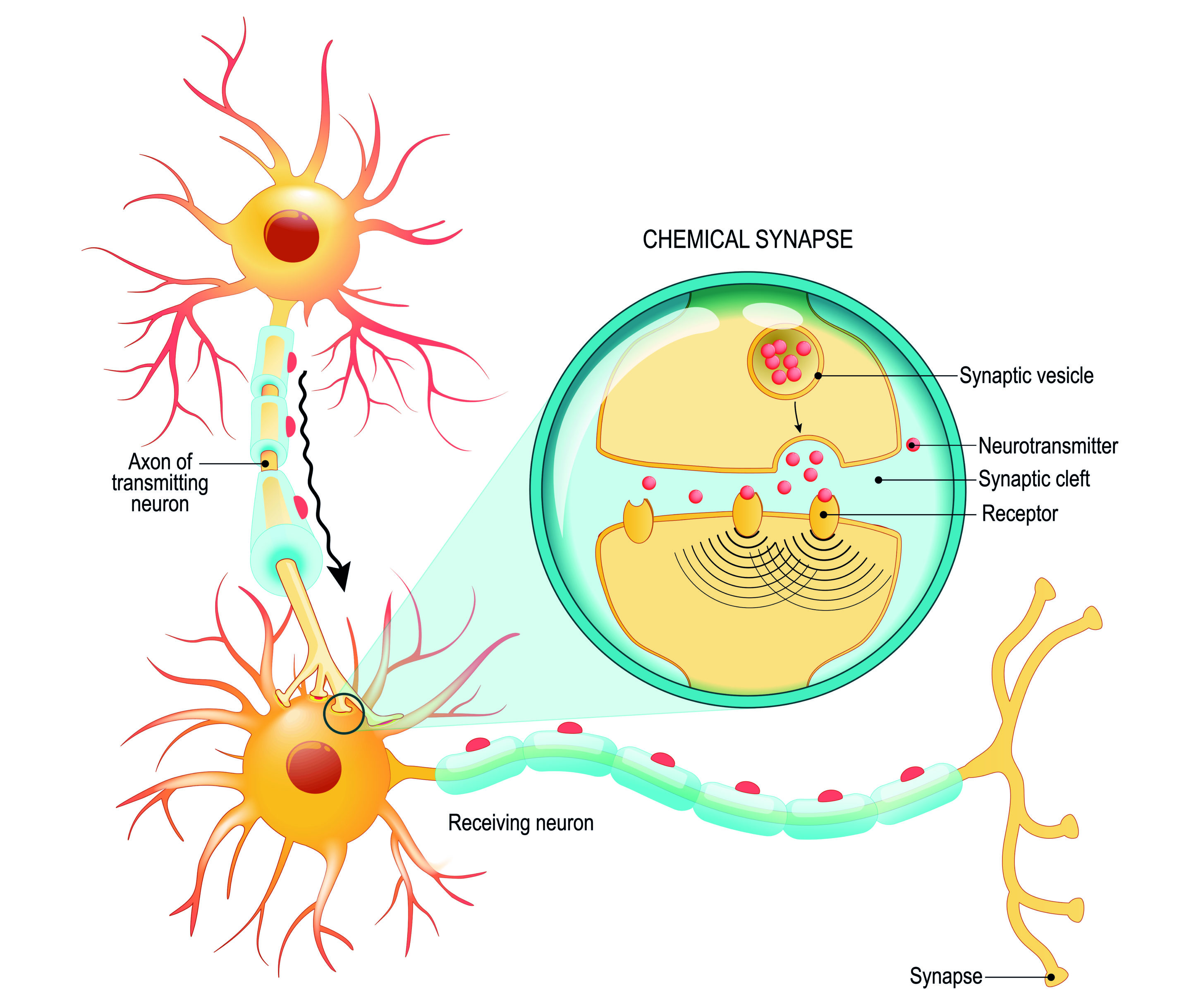
I synapsen frisätts ämnen kallade signalsubstanser som fäster på intilliggande nervcell. På så sätt sprids en nervsignal vidare.
Ryggmärgen
Ryggmärgen är 1 – 1,5 cm tjock och består av nervcellskroppar (kallad grå substans) och nervtrådar (som tillsammans med omgivande stödjeceller kallas vit substans). Den ligger skyddad innanför ryggraden och kan liknas vid en kabel vars uppgift är att ta emot och skicka vidare nervsignaler mellan hjärnan och resten av kroppen. En skada på ryggmärgen kan hindra nervsignalerna att skickas vidare vilket kan resultera i förlamning och förlust av känseln i olika delar av kroppen.
Hjärnan tolkar signalerna
Signalerna från kroppens olika delar som leds via ryggmärgen når hjärnan där de bearbetas och tolkas. Hjärnan gör oss därmed medvetna om vad vi upplever. Om vi t ex bränner oss på spisplattan är det först när nervsignalerna når hjärnan som vi upplever smärtan. Hjärnan skickar också ut signaler om hur kroppen ska reagera på upplevelsen.
Ryggmärgen sköter kroppens reflexer
Ibland räcker det att en signal når ryggmärgen för att kroppen ska reagera. I ryggmärgen aktiveras då något som kallas för reflexbåge, som skickar ut ett svar på den inkommande signalen med en gång. Signalen behöver alltså inte nå hjärnan först och det innebär att reaktionen kan ske snabbare än om den skulle ha behövt tolkas av hjärnan först. Sådana reaktioner kallas för reflexer de fyller en viktig funktion för att skydda kroppen mot skador. I exemplet med spisplattan drar du undan handen innan nervsignalen nått hjärnan och du blivit medveten om värmen och smärtan.
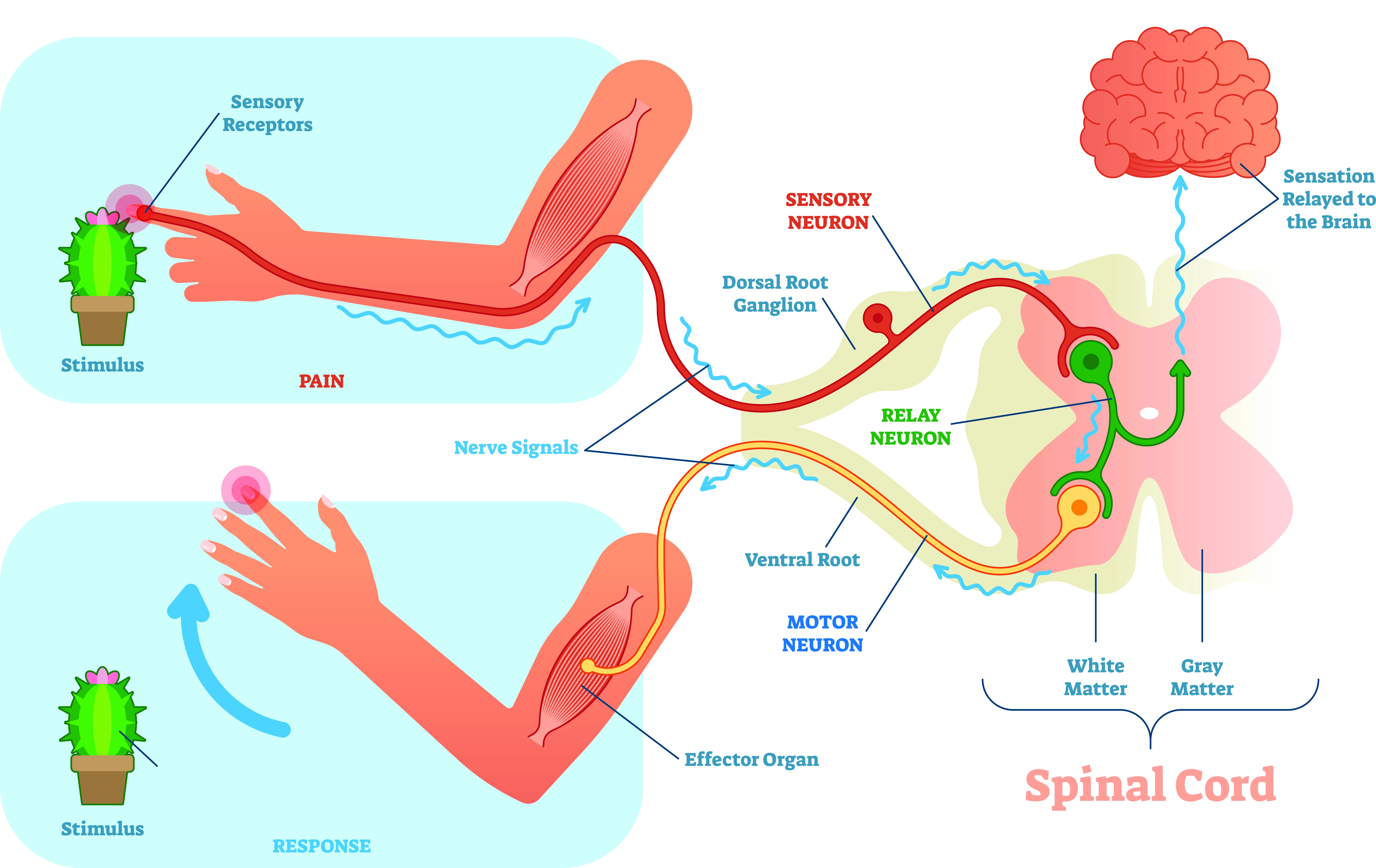
Reflexbågen. Vi drar undan handen från det som orsakar oss smärta innan signalen nått hjärnan och vi blivit medvetna om smärtan.
Perifera nervsystemet
Nervtrådarna i det perifera nervsystemet ligger i buntar. Nerverna skickar vidare information mellan det centrala nervsystemet och resten av kroppen.
Det finns tre grupper av nerver i det perifera nervsystemet:
- Hjärnnerver
- Ryggmärgsnerver
- Autonoma nerver – som inte går att styra med viljan.
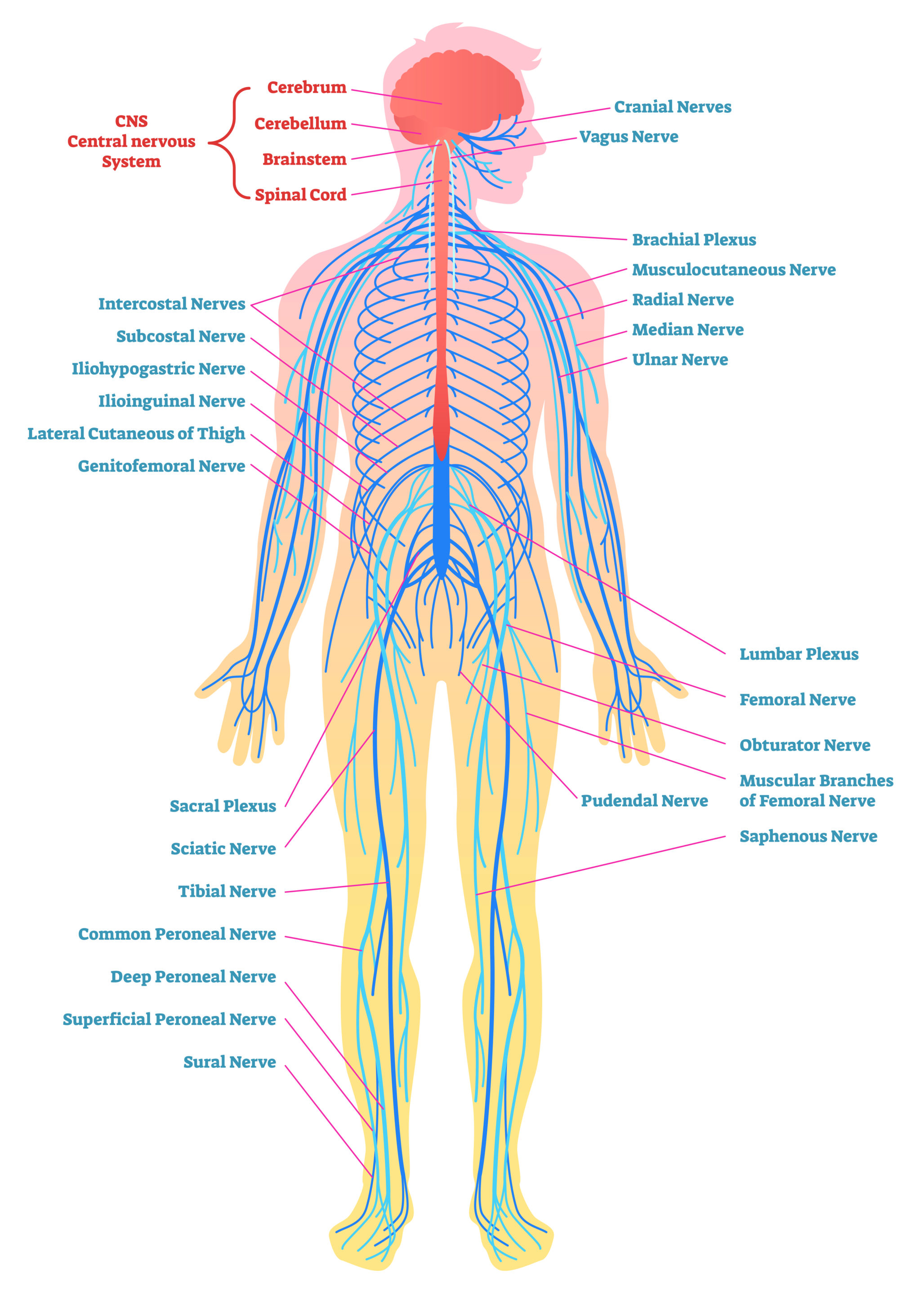
Perifera nervsystemet
- Hjärnnerver
Hjärnnerverna utgörs av tolv par nerver som alla har sina cellkroppar i hjärnan eller hjärnstammen. Hjärnnerverna har följande uppgifter:
– Luktnerven leder information från näsans slemhinna till luktcentrum i hjärnan.Synnerven leder synintryck från näthinnan till syncentrum i hjärnan.
– Tre par hjärnnerver går till ögonens muskler. Nerverna leder impulser till de små musklerna på ögonglobens utsida och gör att vi kan titta uppåt, nedåt och åt sidorna. Nerverna drar även ihop pupillen och gör att linsen som sitter i ögat kan bryta ljuset.
– Trillingnerven är den största hjärnnerven. Den tar emot signaler om känsel från ansiktet. Den leder också signaler till musklerna du använder när du tuggar.
– Ansiktets rörelsenerv leder impulser till ansiktets muskler, tårkörtlarna och två av spottkörtlarna. Dessutom förmedlar nerven smak som registreras på tungans främre del.
– Nerven för hörsel och balans leder information från innerörat till hjärnan.
– Nerven för tunga och svalg leder information till de muskler som gör att du sväljer. Den tar även emot information om smak från tungans bakre del och känsel i svalget.
– Nerven för lunga och mage styr bland annat struphuvudet, hjärtat, lungorna, magsäcken och tarmarna.
– Den så kallade hjälpnerven förmedlar impulser till kappmuskeln och sneda halsmuskeln. Kappmuskeln är den muskel som bland annat lyfter på axlarna. Den sneda halsmuskeln är den muskel som roterar huvudet åt sidorna och som böjer huvudet framåt.
– Tungans nerv styr rörelserna i tungan.
- Ryggmärgsnerver
Ryggmärgen är uppdelad i 31 delar som kallas för segment. Från varje segment går det ut två ryggmärgsnerver – en på höger och en på vänster sida – till kroppens olika muskler och till huden.
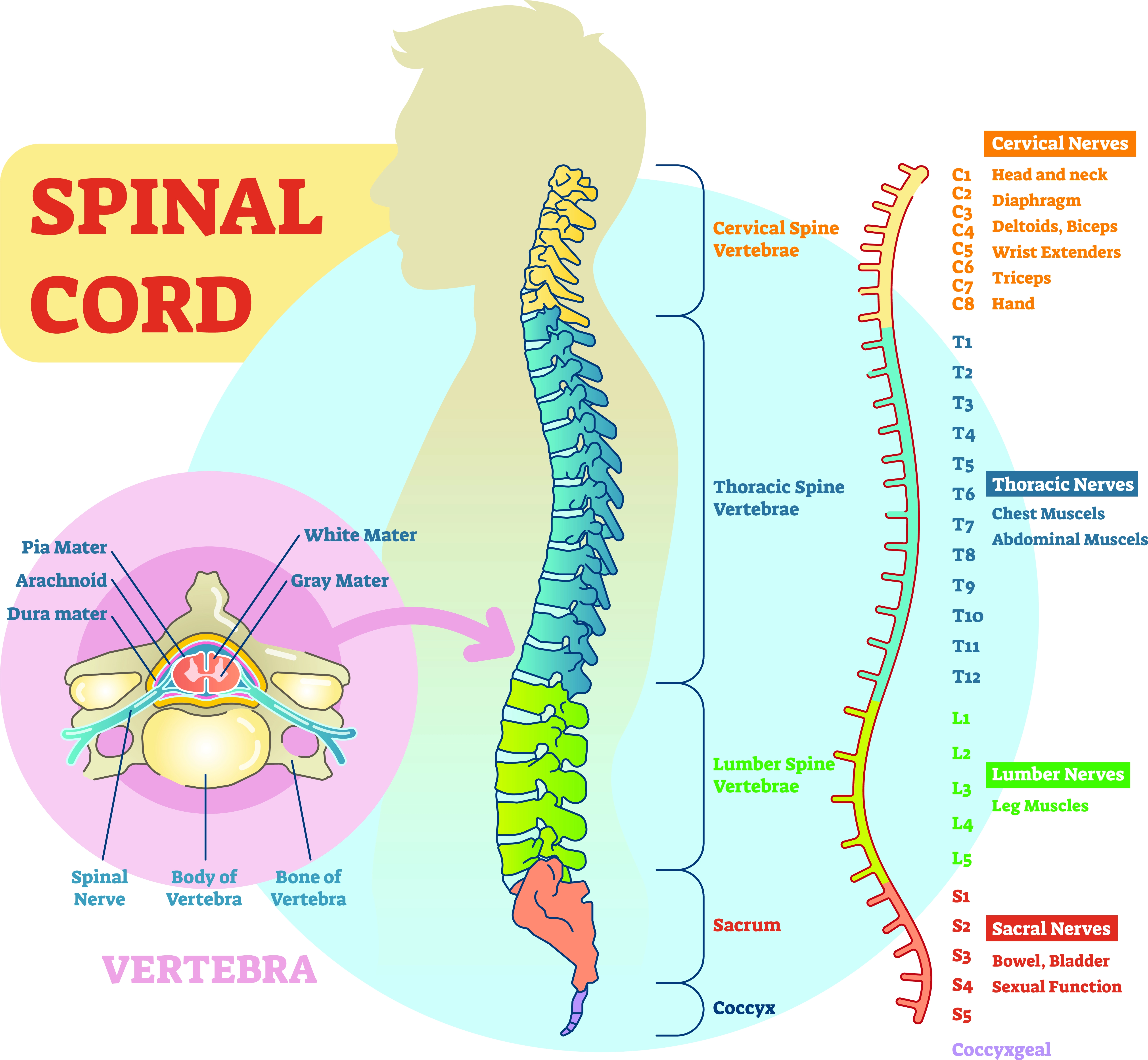
Ryggmärgen skyddas innanför ryggraden och är uppdelad i segment.
Några exempel på ryggmärgsnerver:
– Ischiasnerven är kroppens största och längsta nerv. Den går från nedre delen av ryggmärgen ända ut i stortån.
– Medianusnerven går från ryggmärgen till delar av handen. Denna nerv kan ibland komma i kläm vid handleden och orsaka så kallat karpaltunnelsyndrom.
– Ulnarisnerven leder impulser till handens små muskler. Den går runt armbågen och kan komma i kläm när armbågen stöts till. Det brukar kallas att du får en änkestöt.)
- Autonoma nervsystemet
De nerver som styr inre organ kan inte påverkas av viljan. Det gäller till exempel nerver som styr hjärtats arbete, andningen, blodtrycket, tarmarnas rörelser samt urinvägarnas och könsorganens funktioner. Dessa nerver hör till det självstyrande nervsystemet, kallat det autonoma nervsystemet.
Det autonoma nervsystemet delas i sin tur in i två delar:
- Sympatiska nervsystemet
- Parasympatiska nervsystemet
1. Sympatiska nervsystemet förbereder kroppen för flykt eller kamp.
Det sympatiska nervsystemet sätts igång när kroppen behöver använda sina krafter. Det kan till exempel vara när du blir stressad eller rädd. Kroppen förbereder sig för att fly eller slåss.
Det sympatiska nervsystemet påverkar kroppen på följande sätt:
– Nivån av stresshormonerna adrenalin och noradrenalin ökar.
– Pulsen ökar.
– Hjärtat pumpar kraftigare.
– Blodflödet till musklerna ökar, medan det minskar till hud och inälvor.
– Blodtrycket ökar.
– Luftrören vidgas så att det går lättare att andas.
– Blodsockernivån ökar så att du får extra energi.
– Pupillerna utvidgas.
– Du svettas mer.
– Tarmrörelserna minskar.
– Matsmältningen går långsammare.
2. Parasympatiska nervsystemet är mest aktivt vid vila och i lugna situationer då kroppens reserver byggs upp.
Det parasympatiska nervsystemet påverkar kroppen på följande sätt:
– Pulsen minskar.
– Hjärtats pumpar med mindre kraft.
– Blodtrycket sjunker.
– Luftrören dras ihop.
– Pupillerna dras ihop.
– Mängden saliv i munnen ökar.
– Tarmrörelserna ökar.
– Matsmältningen ökar.
– Du kan kissa och bajsa.
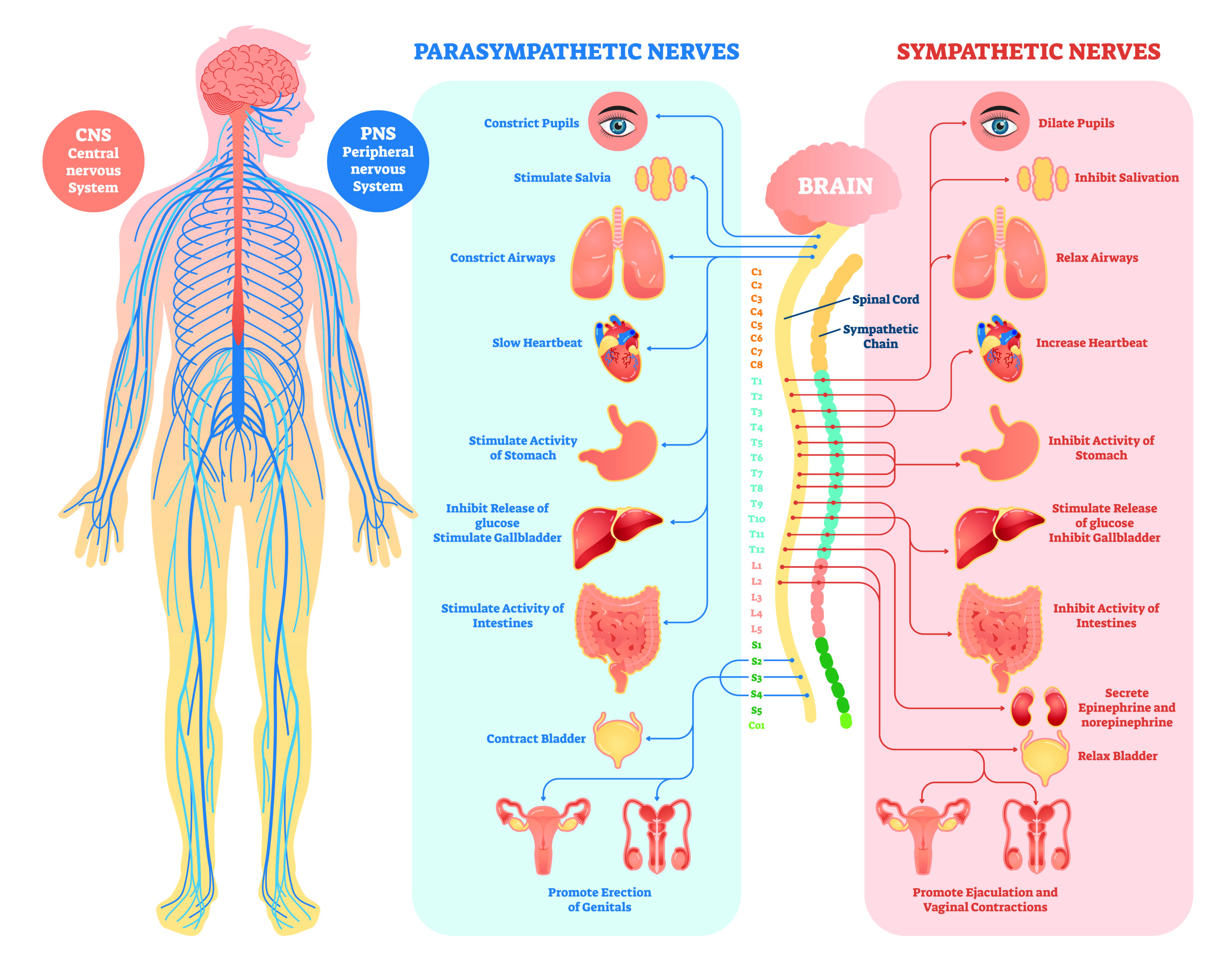
Parasympatiska och sympatiska nervsystemet
Vad skiljer det centrala nervsystemet från det perifera?
En nervtråd som gått av i det perifera nervsystemet kan växa ut igen, men en hel nervcell kan inte dela sig och bilda nya celler. Det innebär att det centrala nervsystemet inte kan läka såsom nervtrådar i det perifera kan. Forskare försöker komma på hur man ska kunna få nervceller att repareras och dela sig, b la genom studier av stamceller.
Tidigare blogginlägg
Stamcellstransplantation vid tetraplegi
Stamcellstransplantation vid tetraplegi
Publicerad 2020-02-25
Bakgrund
En traumatisk ryggmärgsskada förorsakas av någon form av våld (trauma) mot ryggmärgen. I det akuta skedet orsakar detta blödningar. Efter det dör nervceller i skadeområdet och hålrum bildas där cellerna funnits. Nervtrådarnas yttre skikt av myelin bryts ned och det bildas ärrvävnad.
I det kroniska stadiet ersätts ryggmärgens nervceller (även kallad grå substans) av hålrum eller av ärrvävnad uppbyggd av kollagen. Kvar blir oftast en kant av nervcellstrådar (dessa kallas axon eller vit substans).
Celltransplantation
En metod som studeras för att försöka reparera skadad ryggmärg är transplantation av celler som kan motverka eller reparera dessa skador.
Det amerikanska bioteknikföretaget Lineage Cell Therapeutics använder sig av nedfrusna celler odlade från humana embryonala stamceller. Celllinjen kallas AST-OPC1, där OPC står för oligodendrocyt progenitorceller. De mognar i ryggmärgen till oligodendrocyter.
(Man kan läsa mer om vad en stamcell är i det tidigare inlägget Celltransplantation efter ryggmärgsskada).
Det centrala nervsystemet är i huvudsak uppbyggt av två typer av celler: nervceller och stödjande gliaceller. Oligodendrocyter är en sorts stödjande gliacell. De producerar ett isolerande hölje kallat myelin runt nervcellernas utskott som är nödvändigt för att de elektriska signalerna ska kunna transporteras längs med nerverna. Man kan jämföra en nervcells myelinskikt med isoleringen runt en elektrisk kabel.

Oligodendrocyt som producerar myelin.
Man har efter djurstudier och in vitro studier (studier i labb, provrör) identifierat tre funktioner hos AST-OPC1-cellerna:
- De producerar nervtillväxtfaktorer
- De bidrar till remyelination, dvs. återbildande av nervernas skadade myelinskikt
- De hjälper till att starta nybildandet av blodkärl
Samtliga mekanismer är avgörande för överlevnad och återväxt av nerver och för att nervimpulser ska kunna transporteras längs med nervcellstrådarna vid skadeområdet.
Studie med transplanterade AST-OPC1
Lineage Cell Therapeutics (som förr hette Asterias Biotherapeutics) genomför en studie där AST-OPC-1-celler transplanteras till ryggmärgen hos personer med cervikal ryggmärgsskada på nivå C5-C7. Cellerna ges 21- 42 dagar efter skadan.
Ett första försök gjordes 2014 på fem personer för att säkerställa säkerheten. Dosen som gavs var för låg för att ge resultat men metoden konstaterades säker. Detta försök gjordes på personer med skada på thorakal nivå.
Det andra försöket påbörjades 2016 och har utförts på ett tiotal olika center i USA. Totalt har 25 personer indelade i fem grupper fått olika koncentration av cellerna injicerade i ryggmärgen. Personerna har i samband med transplantationen fått läkemedel för att hämma det egna immunförsvaret (för att undvika frånstötning av de främmande cellerna).
Grupp 1-3 har komplett cervikal skada. De har fått 2 respektive 10 och 20 miljoner celler. Grupp 4-5 har inkomplett cervikal skada och har fått 10 respektive 20 miljoner celler. Patienterna har följts under ett år med neurologiska tester och MRI-röntgen. En långsiktig 14-årig uppföljning görs också.
Resultat
I januari 2019 rapporterades resultat då samtliga deltagare följts upp under 12 månader:
- 96% av deltagarna fick förbättrad motorisk funktion i övre extremiteter på ena sidan av kroppen.
- 32% av deltagarna fick förbättrad motorisk funktion i övre extremiteter på båda sidorna av kroppen.
Deltagarna själva rapporterade förbättrad kontroll av överkroppen och förbättrad förmåga att självständigt klara vardagliga aktiviteter. Särskild förbättring sågs i användningen av händer, fingrar och armar.
- Hos 96% av deltagarna kunde man vid undersökning med magnetkamera se vävnadsmatrix vid skadeområdet.
Detta är positivt eftersom det tyder på att de transplanterade cellerna växer (eng. engrafting) vilket förhindrar hålrum med ärrvävnad som följd. Ärrvävnad uppstår ofta efter ryggmärgsskada och förvärrar skadan.
Rapporter visar att förbättringar i övre extremiteter som armar, händer och fingrar är den enskilt mest betydelsefulla förbättringen för personer med tetraplegi, eftersom även små förbättringar kan ha stor betydelse för självständighet, livskvalitet och vårdkostnader.
I november 2019 rapporterades ytterligare en uppföljning. En del av deltagarna hade då följts upp under två år och resultaten är fortsatt goda.
Företaget planerar nu ytterligare kliniska studier med cellerna för att förfina och optimera metod, dosering och tid för transplantation. Företaget hoppas också att man på sikt ska kunna utöka behandlingen till att även användas vid neurodegenerativa sjukdomar som MS och stroke.
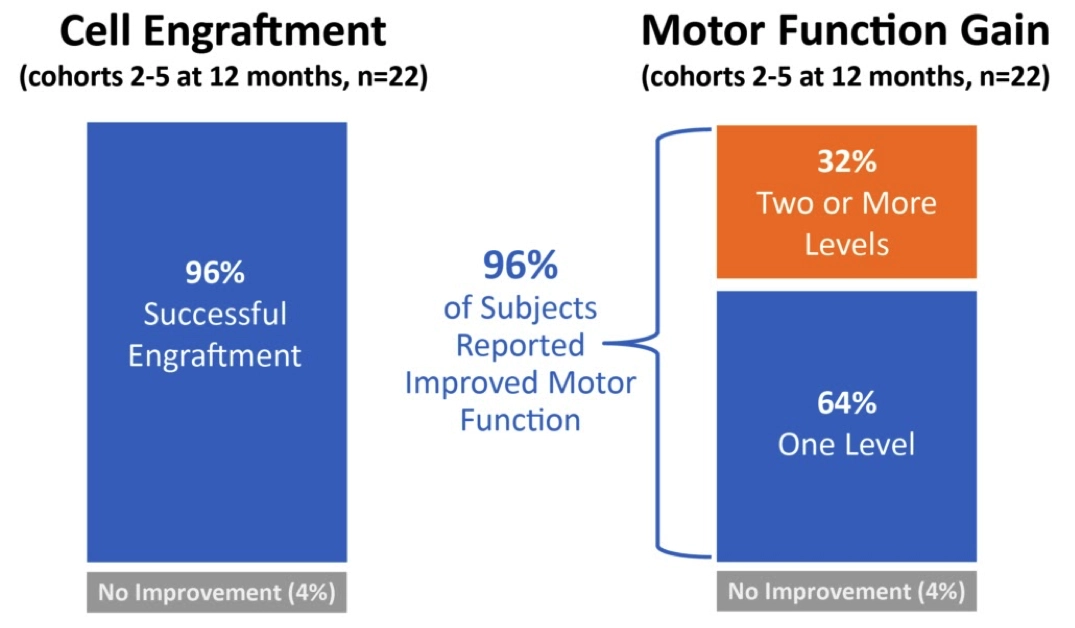
Diagram över resultat vid 12 månaders uppföljning. n= antal personer
Uppdatering – Svensk studie med implantat i ryggmärgen
Publicerad 2019-11-20
Denna uppdatering syftar till det tidigare inlägget ”Svensk studie med implantat i ryggmärgen”.
Bioartic meddelar att de avbryter studien med implantat i ryggmärgen, då de första 9 studiedeltagarna nu utvärderats efter 18 månaders rehabilitering i lokomaten. Utvärderingen visar att ingen av studiedeltagarna uppvisat önskad effekt i form av elektriska impulser som passerar över skadeområdet — vilket är en förutsättning för att kunna återfå motorisk funktion. Bioartic stoppar därför rekryteringen av nya studiedeltagare. Vd Gunilla Osswald kommenterar beslutet: ”Även om det är nedslående att SC0806-behandlingen inte har den effekt som de prekliniska resultaten indikerade så har vi med Fas 1/2-studien bidragit till ökad kunskap om ryggmärgsskadade patienter. Vi kommer att avsluta studien på ett kontrollerat och ansvarsfullt sätt och se till att värdefull kunskap som samlats in sprids till övriga forskare världen över”.
Celltransplantation Efter Ryggmärgsskada
Publicerad 2018-03-16
Forskning som syftar till att lösa gåtan om hur man kan ”laga” en trasig ryggmärg tar sig an problemet från lite olika angreppspunkter. I de två tidigare texterna beskrivs metoder som använder sig av implantat för att få nerverna att läka ihop och av elektrisk stimulering för att aktivera nervceller.
En annan metod är att transplantera celler till det skadade området. En del av dessa studier använder sig av stamceller. Därför är det bra att klargöra vad en stamcell egentligen är.
Vad är en stamcell?
Stamceller är omogna icke-specialiserade celler som kan genomgå ett obegränsat antal celldelningar och har förmågan att mogna till flera olika celltyper. Detta gör dem väldigt intressanta för forskningen.
Den stamcell som uppstår då ett ägg blir befruktat och som har potential att bilda vilken cell som helst – inklusive moderkaka – kallas totipotent stamcell.
Den sorts stamcell som kan mogna till vilken celltyp som helst i den vuxna kroppen – men alltså inte till moderkaka – kallas pluripotent stamcell.
Andra stamceller kan mogna till närbesläktade celltyper som hittas i samma organ eller vävnad; de kallas multipotenta stamceller.
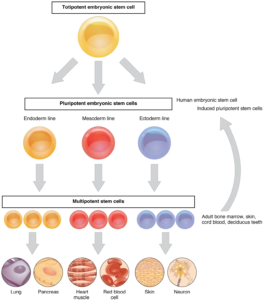
Illustrationen nedan är från Anatomy & Physiology, Connexions webbplats. Nedladdad från Wikimedia Commons. 2018.
Olika sorters stamceller
Embryonala stamceller: Alla celler i kroppen härstammar från den stamcell som kan mogna till vilken cell som helst: det befruktade ägget. Den är totipotent och kan även bilda moderkaka. Fem till sju dagar efter befruktningen har embryot utvecklats till en mjuk klump av celler (blastocyst). Från dess inre är det möjligt att hämta celler som går att odla i laboratorium. Dessa kallas för embryonala stamceller och kan bilda alla celler som finns i den vuxna människokroppen – de är pluripotenta.
Embryonala stamceller brukar hämtas från befruktade ägg som blivit över från provrörsbefruktningar.
Fosterstamceller: Förutom embryonala stamceller finns det stamceller som tas från aborterade foster eller ur det blod som kan tas via dess navelsträng. Dessa celler är multipotenta; dvs. kan ge upphov till närbesläktade familjer av celler. Tex kan stamcellerna från fostrets nervsystem bilda de olika typerna av nervceller, och stamcellerna från navelsträngen kan ge olika sorters blodceller.
Adulta stamceller: Det finns även adulta (vuxna) stamceller i den vuxna organismen. De har till uppgift att underhålla och reparera kroppens vävnader och organ. Adulta stamceller är svåra att påvisa och antalet är mycket litet. De finns i flera vävnadstyper; bla i benmärgen och i begränsad omfattning i hjärnan. De flesta är multipotenta och kan således ge upphov till närbesläktade celler. De som finns i benmärgen kan bilda ben-, brosk-, fett- och muskelceller och har tex. använts för att få skadad hjärtvävnad att läka.
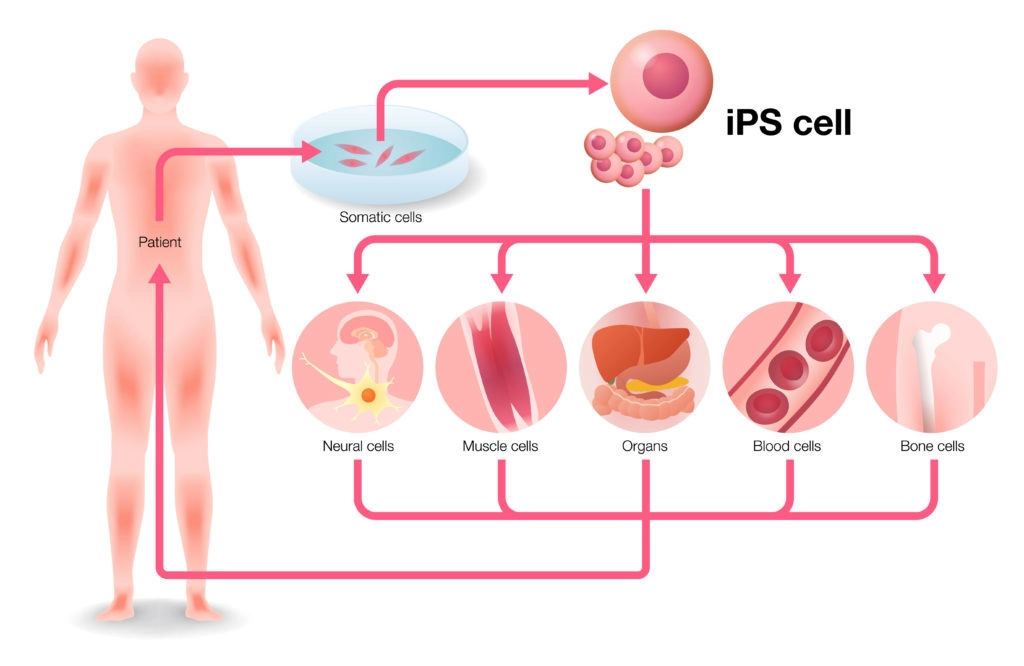
IPS-celler: 2007 upptäckte man att man kan få vanliga hudceller från en människa att tillbakabildas till stamceller med samma potential som embryots. De kallas inducerade pluripotenta stamceller (IPS-celler).
Fördelen med dessa är; förutom att man slipper den etiska problematiken med att ta celler från ett embryo; att IPS-celler har samma gener som den individ de hämtas från och därför i teorin lämpar sig fint för transplantation. Nackdelen är att metoden för att ta fram dem kan ge en risk för cancer. (2)
De celler man hittills fokuserar på i studier för att läka en ryggmärgsskada är:
(1)
1. Schwann-celler: en typ av gliaceller (stödjeceller) som finns runt nervceller i det perifera nervsystemet; dvs. utanför hjärnan/ryggmärgen (som utgör det centrala nervsystemet). Schwannceller har flera viktiga funktioner för nervcellerna varav en är att tillverka det isolerande myelinskikt (en slags fettskida) runt axonen (nervtrådarna) som är nödvändigt för nervimpulsers fortledning. Vid en skada på perifera nerver är Schwannceller nödvändiga för att axonen ska växa ut igen.
2. Olfaktoriska stödjeceller: Gliaceller som återfinns i luktorganet och omger luktnervercellers axon (på samma sätt som Schwannceller omger perifera nervers axon). Olfaktoriska stödjeceller har flera funktioner som främjar axonernas återväxt och har med framgång testats på råttor med ryggmärgsskada (3)
3. Adulta stamceller från vuxen benmärg (multipotenta)
4. Neurala stamceller isolerade från centrala nervsystemet med förmåga att differentiera till nervceller och gliaceller.
5. Embryonala stamceller med förmåga att differentiera till vilken celltyp som helst (pluripotenta)
Hur transplanterade celler kan förbättra funktion efter ryggmärgsskada:
(1)
Trauma på ryggmärgen triggar igång en kaskad av sekundära skador på nervcellerna. En förklaring till varför celltransplantation förbättrar funktion efter ryggmärgsskada är att de transplanterade cellerna skyddar nervcellerna från dessa sekundära skador.
Cellerna skyddar nervcellerna genom en rad olika mekanismer;
1. Genom att utsöndra ämnen kallade trofiska faktorer eller cytokiner som i sin tur förbättrar cellernas överlevnad, reglerar den förändring av gliaceller som annars sker och som kan ge upphov till ärrbildning, påverkar inflammatoriska processer och förbättrar återbildning av blodkärl.
2. Genom att motverka förlust av blodkärl och/eller förbättra nybildning av blodkärl. Efter en skada på ryggmärgen sker en stor förlust av fungerande blodkärl vilket orsakar syrebrist och celldöd i och omkring det skadade området. Transplanterade celler tycks kunna bidra till att återställa syre och näringsämnen till vävnad kring skadeområdet.
3. Genom att påverka immunsystemet och förhindra inflammation. Immunsystemet är komplext och en del inflammatoriska processer som sätts igång efter en skada på ryggmärgen är nödvändiga för reparation; medan andra inflammatoriska processer kan orsaka ökad skada på vävnaden. Transplanterade celler kan verka positivt på skadan genom att öka de positiva inflammatoriska processerna och minska de negativa.
4. Genom att förbättra återväxten av axon (nervtrådar). Den primära anledningen till förlusten av funktion efter en ryggmärgsskada är att de centrala nerverna i ryggmärgen inte kan förmedla signaler eftersom nervtrådarna ”gått av”. Återbildandet av axonen hindras bla. genom att ärrvävnad uppstår vid skadan, av att myelin-skiktet runt axonen skadats och av det faktum att nerver i centrala nervsystemet hos vuxna däggdjur i princip inte kan växa tillbaka (särskilt inte då axonerna gått av). Transplanterade celler kan gå in och påverka dessa processer; t.ex. genom:
a) att möjliggöra bildandet av ”broar”:
Den starkast etablerade förklaringen till hur transplanterade celler kan underlätta axoners tillväxt är genom att cellerna bildar ”broar” över skadeområdet. En bro definieras som en struktur uppbyggd av transplanterade celler som överbrygger skadeområdet och på vilken axoner kan växa. De transplanterade cellerna utsöndrar även ämnen som främjar tillväxt. Samtliga av de celltyper beskrivna i texten ovan kan bilda broar efter ryggmärgsskada och brostrukturen kan förstärkas genom att kombinera cellerna med biomaterial och tillväxtfaktorer.
Ett problem är att nervceller i olika nervbanor i ryggmärgen uppvisar stora skillnader i förmågan att växa över broar. T.ex. verkar sensoriska uppåtgående nerver (nerver som förmedlar känsel från kroppens olika delar upp till hjärnan) kunna växa ganska bra över broar medan nedåtgående nerver i den kortikospinala banan (nerver som går från hjärnan ut till muskulaturen och förmedlar motorik) tycks ha svårare att växa över broar.
b) att påverka bildandet av ärrvävnad:
Efter en skada på ryggmärgen aktiveras en typ av gliaceller/stödjeceller kallade astrocyter som bl.a. bidrar till att bilda ärrvävnad vid skadeområdet. Ärrvävnaden tycks ha både positiva och negativa effekter; den skyddar kringliggande vävnad från tex. inflammatoriska celler i skadeområdet men försvårar även axoners återväxt över skadeområdet.
c) att underlätta återbildning av myelin:
Myelin-skiktet på nerver i centrala nervsystemet bildas av gliaceller kallade oligodendrocyter (Dessa fyller alltså samma funktion som Schwanncellerna fyller i det perifera nervsystemet). Myelin-skiktet kan jämföras med ett isolerande fetthölje runt nervernas axon som gör det möjligt för nervsignaler att transporteras. Skiktet förstörs vid en skada på ryggmärgen och man har sett att funktion i ryggmärgen kan förbättras genom att ersätta förlorade oligodendrocyter och förstört myelin.
Genom att transplantera Schwannceller eller stamceller som kan ge upphov till oligodendrocyter kan man eventuellt förbättra återbildningen av myelin efter en ryggmärgsskada.
Ett amerikanskt biotech-företag som forskar på en typ av stamceller som ger upphov till oligodendrocyter har genomfört kliniska försök på människor med ryggmärgsskada på både thorakal och cervikal nivå. (4,5) Man kan läsa mer om deras forskning i ett kommande blogginlägg.
Var står vi idag?
Sammanfattningsvis har majoriteten av studier av celltransplantation efter ryggmärgsskada gjorts på djur och det kvarstår ännu att ta reda på mer angående verkningsmekanism, effekt och säkerhet innan man kan ta dem vidare till människa.
Det pågår idag flera kliniska studier och området innebär en viktig del av framtida forskning inom ryggmärgsskador, men ännu har man inte lyckats hitta så många faktiska förklaringsmodeller till varför en behandling ger effekt utan snarare bara sett att det gör det. Man behöver även utöka storleken på grupperna studierna görs i för att de ska ge tillförlitliga resultat. Tyvärr har de begränsade fynd som hittats gett bränsle åt stamcells-turism till kliniker runt om i världen som erbjuder cellbehandlingar utan vetenskapligt underbyggda resultat.
Celltransplantation som behandling för ryggmärgsskador utgör ett spännande område för framtida forskning, men en hel del återstår ännu innan någon behandling med bevisad effekt finns ute i klinik.
Ref
1. https://www.ncbi.nlm.nih.gov/pubmed/28440805
2. http://www.kmagasin.se/
3. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4886956/
4 https://scistar-study.com/about-scistar-study/
5. https://www.globenewswire.com/news-release/2019/01/24/1704757/0/en/Asterias-Provides-Top-Line-12-Month-Data-Update-for-its-OPC1-Phase-1-2a-Clinical-Trial-in-Severe-Spinal-Cord-Injury.html
Svensk studie med implantat i ryggmärgen
Publicerad 2017-09-05
Forskare verksamma vid Karolinska Institutet har tillsammans med biotech-företaget BioArctic Neuroscienceinlett ett EU-finansierat forskningsprojekt som bygger på att man ersätter en bit av ryggmärgen med ett kalciumsulfatimplantat som genomborrats med 12 kanaler i vilka man placerar perifera nerver (se förklaring i texten nedan).
Just nu pågår den här studien som engagerar försökspersoner med en komplett ryggmärgsskada i bröstryggen. Implantatet som är gjort av kalciumsulfat bryts ner av kroppen efter ett par veckor. Det kan liknas vid en 5-8 mm tjock och 15-20 mm lång vinkork som har kanaler som korresponderar med den arkitektur som representeras av ryggmärgens nervbanor – såsom de löper inuti ryggmärgen.
Under ett kirurgiskt ingrepp tas den skadade delen av ryggmärgen bort och ersätts av implantatet. I kanalerna placeras nerver som tas från underbenet på försökspersonen. Dessa nerver kallas perifera nerver och skiljer sig från nerver som tillhör det centrala nervsystemet på flera sätt.
Till skillnad från nerver i centrala nervsystemet kan perifera nerver ”regenerera”. Det betyder att perifera nerver kan växa ut i det tidigare skadade området som förlorat motorik eller känsel. De perifera nerverna växer ut i det ”skelett” som utgörs av den tidigare fungerande nerven. De nerver som placeras i implantatets kanaler kan alltså inte läka ihop med de centrala nerverna men är tänkta att fylla denna guidande funktion som det skelett de perifera – här centrala – nerverna kan växa längs med.
Innan implantatet placeras i ryggmärgen dränks det in med en tillväxtfaktor kallad Fgf-1 (fibroblast growth factor 1). Denna behövs för att nervtrådar ska kunna växa. Tanken är att i implantatet skapa en så gynnsam miljö som möjligt för nerverna att växa i så att de skadade nerverna i ryggmärgen ska hitta tillbaka till varandra.
Man har testat metoden på råttor vars ryggmärg skurits av med lyckat resultat. Råttornas ryggmärg har delvis återfått sin tidigare funktion avseende t.ex. partiell gångförmåga.
 Efter operationen får försökspersonerna i studien gångträna i en slags gångrobot kallad lokomat; en timme, tre gånger i veckan i 18 månader. Tanken med denna träning är att återaktivera det program som sitter i lillhjärnan och som styr vårt gångmönster.
Efter operationen får försökspersonerna i studien gångträna i en slags gångrobot kallad lokomat; en timme, tre gånger i veckan i 18 månader. Tanken med denna träning är att återaktivera det program som sitter i lillhjärnan och som styr vårt gångmönster.
Parallellt med de personer som fått implantatet får ett antal kontrollpersoner genomgå enbart enbart träningsdelen av studien. Detta för att kunna avgöra vilka eventuella effekter som beror på implantatet och vilka som beror på träningen i lokomaten.
Studien är tänkt att utföras under flera år och totalt inkludera 27 försökspersoner. Den sker i tre omgångar med 9 personer i varje grupp; 6 personer som får implantat och 3 kontrollpersoner. Deltagarna rekryteras från Sverige, Finland och eventuellt ytterligare något nordiskt land. Hittills är 6-7 personer med i studien.
Kriterier för att inkluderas i studien är bla. att personen varit skadad i över ett år men inte mer än 4-5 år, att skadan är på bröstkotenivå, är komplett samt att ärret (skadeområdet) inte är längre än 3 cm. Detta beror på att implantatet inte kan göras hur långt som helst.
Under studiens gång görs kontinuerligt neurofysiologiska och fysioterapeutiska tester för att mäta eventuella förändringar.
Studien startade kliniskt i januari 2016 och ännu har inga resultat redovisats.
Epidural elektrisk stimulering - elektroniskt implantat i ryggmärgen
Publicerad 2017-10-03
Epidural elektrisk stimulering – EES – är en metod som innebär att man stimulerar ryggmärgen via elektroder som placeras över ryggmärgen i det så kallade epidurala mellanrummet, mellan ryggraden och ryggmärgen. Än så länge har metoden endast använts över ryggmärgens nedre del. Elektroderna är kopplade till en batteridriven stimulator som placeras under huden. Den elektriska strömmen kontrolleras via en fjärrkontroll utanför kroppen. På så vis kan man aktivera motoriska nervbanor i ryggmärgens nedre del som kontrollerar muskulatur i underkroppen.
Metoden har gett positiva resultat hos försökspersoner som kunnat röra sina ben, stå upp och utföra rörelser som liknar gångmönster med hjälp av stimuleringen och forskarna menar att EES i kombination med fysioterapi kan vara en metod för att stärka nervsignalering över skadeområdet vid i första hand inkompletta ryggmärgsskador.
2014 publicerades en studie i ”Brain- Journal of neurology” av forskare verksamma vid University of Louisville, Kentucky, USA, där fyra ryggmärgsskadade personer (nivå C7-T5), varav två med komplett skada, viljemässigt lyckats utföra rörelser med hjälp av EES. Samtliga personer hade varit skadade i minst 2 år. (1)
Deltagarna fick träna i en gångrobot, en s.k. lokomat tillsammans med fysioterapeut vid minst 80 tillfällen under minst 19 veckor innan implantatet opererades in.
Neurofysiologiska tester som TMS, SEP och ASIA gjordes både före och efter denna träning för att kontrollera eventuella förändringar i motorik och känsel.
När implantatet var på plats följde en testperiod för att ställa in lämplig frekvens och intensitet på den elektriska strömmen. Personerna ombads vid testerna att försöka utföra specifika rörelser som att sträcka ut ankeln samtidigt som den elektriska stimuleringen var på. Tre av fyra försökspersoner lyckades viljemässigt med detta redan under testperioden.
Därefter fick deltagarna ett en-timmas träningsprogram att utföra i hemmet sju dagar i veckan. De fick då ligga på rygg och träna att röra hela benet, ankeln och tårna. De kunde själva reglera EES styrka med hjälp av fjärrkontroll för att uppnå bästa resultat.
Parallellt med detta tränade de ståträning (17-23 veckor) och gångträning (17-20 veckor) tillsammans med fysioterapeut. Ståträningen och den dagliga träningen liggande på rygg fortsatte därefter från hemmet tills utvärdering gjordes.
Träningen gav resultatet att deltagarna kunde utföra rörelserna med allt större kraft och med hjälp av allt svagare elektrisk stimulering.
Vid utvärderingen lyckades samtliga deltagare utföra viljemässiga rörelser under stimulering med EES. En deltagare med inkomplett skada kunde även utföra rörelserna utan den elektriska stimuleringen.
Forskarna poängterar dock att rörelserna deltagarna lyckas utföra har sina begränsningar när det gäller vinster i det vardagliga livet och att de inte kan jämföras med normala rörelsemönster. För att uppnå detta behöver tekniken utvecklas och finjusteras. Deltagarna rapporterar dock att de använder sig av EES-stimuleringen i bål och ben för att öka stabilitet, styrka och uthållighet i vardagen och vid träning. De rapporterar även förbättrad blodcirkulation, temperaturreglering och kontroll av blåsa (5).
En hypotes är att anatomiska nedåtgående nervförbindelser i ryggmärgen kan finnas kvar även hos deltagarna diagnostiserade med komplett skada, men att nervimpulserna inte kan föras vidare längs med dessa nervfibrer p.g.a skador på nervernas myelin-skikt eller på icke fungerande jonkanaler; faktorer som är nödvändiga för att en nervsignal ska transporteras vidare.
Forskarna föreslår att den elektriska stimuleringen från EES förstärker den egna nervsignalen och gör det möjligt för den att transporteras över det skadade området och nå fram till muskulaturen.

Myelin är ett isolerande skikt runt nervernas utskott, axon, som är nödvändigt för att en elektrisk impuls ska kunna transporteras längs med nerven. Myelinet tillverkas av specialiserade celler i nervsystemet och kan jämföras med isoleringen kring en elektrisk ledning. Vid sjukdomen MS förstörs myelinet av kroppens eget immunförsvar och även här förhindras nervsignalerna att komma fram.
I ett aktuellt amerikanskt forskningsprojekt använder man stamceller som utvecklas till den celltyp som tillverkar myelin; oligodendrocyter; i försök att reparera ryggmärgen. (3)
I en studie från 2017 har forskare verksamma vid Mayokliniken i Rochester, Minnesota, USA, i samarbete med forskare vid UCLA , Kalifornien, upprepat resultaten med EES hos en man med paraplegi sedan 3 år tillbaka. Mannen har kunnat röra sina ben, stå upp och utföra rörelser som liknar gångmönster med hjälp av det elektriska implantatet redan efter 2 veckor (8 träningstillfällen). (2)
Innan implantatet fick mannen genomgå intensiv träning med fysioterapeut tre gånger i veckan under 22 veckors tid. Man gjorde under dessa veckor kontinuerliga tester och forskarna såg då förändringar som fick dem att karaktärisera skadan som inkomplett snarare än komplett, då viss nervförbindelse hittades.
De resonerar över svårigheten att med dagens diagnostiska metoder helt fastställa huruvida en skada är komplett eller inte, och över möjligheten att det kan finnas kvar nervförbindelser som helt enkelt är ”tysta” och inte förmår föra vidare nervsignaler även vid diagnostiserade kompletta skador. (1)
Forskargruppen vid University of Louisville, Kentucky, har fått medel från bl.a Wings for Life Spinal cord Research Foundation för att utöka studien med EES-stimulering med 36 försökspersoner och kommer även att titta på eventuella autonoma vinster av EES-behandling såsom kardiovaskulär hälsa, blåskontroll, temperaturreglering samt mag-tarmfunktion. (4).
Ref:
1. https://www.ncbi.nlm.nih.gov/pubmed/24713270
2. https://www.ncbi.nlm.nih.gov/pubmed/28385196
3. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4600489/
4. http://www.biosciencetechnology.com/article/2015/03/epidural-stimulation-shows-promise-spinal-cord-injuries
5. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3361963/

Charlotte bröt ryggen i en fallolycka 2012 då hon var i USA för en jobbintervju och har en komplett ryggmärgsskada från Th9. Hon bor i södra Stockholm, har en medicine magister examen och en bakgrund inom neurovetenskaplig forskning på bl.a. Karolinska institutet.
Hon vill med sin blogg skriva om aktuell forskning inom ryggmärgsskador på ett tillgängligt sätt. Stora intressen är förutom att förstå hur hjärnan fungerar segling, mode, matlagning och att vara ute i skogen med hunden.